Abstract
La Sudden unexpected death in epilepsy è la morte improvvisa, inaspettata, non traumatica di un individuo affetto da epilessia, con o senza evidenza di convulsioni, nella quale l’esame post mortem non evidenzi altre cause del decesso.
Nonostante si tenda a far ricadere in questa fattispecie molti decessi improvvisi in soggetti epilettici, la Letteratura dà precise indicazioni sotto forma di diverse categorie diagnostiche e documenta sempre più come si tratti di una patologia complessa in cui è possibile più di un meccanismo eziologico.
Vi proponiamo la lettura di una recentissima review sull’argomento pubblicata del LICE SUDEP Study Group – per leggere l’intero articolo clicca qui.
. . . .
Sudden unexpected death in epilepsy (SUDEP)
La Unified SUDEP Definition and Classification, proposta da Nashef e colleghi nel 2011, identifica diverse categorie diagnostiche:
- Definite SUDEP: “morte improvvisa, inaspettata, testimoniata o non testimoniata, non traumatica e non dovuta ad annegamento, di un individuo affetto da epilessia, con o senza evidenza di crisi epilettica, non conseguente a stato di male epilettico (=crisi subentranti o crisi di durata >30 minuti) e in cui l’esame post mortale non evidenzi una causa tossicologica o anatomica cui si possa imputare il decesso”.
- a Definite SUDEP Plus: categoria che soddisfa i criteri della ‘definite SUDEP’ ma include la presenza di una patologia concomitante differente dall’epilessia; il decesso può essere attribuito all’effetto combinato dell’epilessia e della ulteriore patologia, senza che questa possa essere idonea autonomamente a cagionare la morte.
- Probable SUDEP/Probable SUDEP Plus: stessi criteri diagnostici della SUDEP ad esclusione del requisito autoptico, perché l’autopsia non è stata eseguita.
- Possible SUDEP: è presente una patologia che entra in diagnosi differenziale quale causa di morte.
- Near-SUDEP/Near-SUDEP Plus: paziente con epilessia che sopravvive dopo rianimazione per almeno 1 ora dopo un arresto cardiorespiratorio che non ha causa strutturale identificabile.
- Not SUDEP: è nota una causa di morte alternativa.
- Unclassified: non sono disponibili informazioni complete, con impossibilità alla classificazione della causa del decesso.
.
Epidemiologia della SUDEP
La SUDEP è la più comune causa di morte epilessia-relata ed è responsabile del 17% dei decessi dei soggetti affetti da epilessia.
L’incidenza della SUDEP varia significativamente a seconda di quale sia la popolazione considerata, collocandosi in un range che va da circa 1 su 10000 pazienti/anno in coorti di pazienti di nuova diagnosi fino a circa 1 su 100 pazienti/anno tra i soggetti con grave epilessia candidati alla chirurgia.
Per questo è importante sapere che esistono dei fattori di rischio, che devono essere tenuti in considerazione per stimare la prognosi. Questi includono:
- politerapia (>3 farmaci antiepilettici);
- scarsa compliance alla terapia farmacologica;
- genere maschile;
- epilessia insorta in giovane età;
- disturbi dello sviluppo;
- convulsioni notturne;
- scarso controllo farmacologico delle crisi comiziali;
- alta frequenza delle crisi (> 50/anno);
- storia di malattia > 30 anni.
Alcuni studi indicano un’alta incidenza nei soggetti epilettici con ritardo mentale e/o disabilità nell’apprendimento (2.1-5.9 decessi / 1000 soggetti all’anno), mentre nei pazienti con epilessia refrattaria alla terapia farmacologica l’incidenza sarebbe pari a 2.2-3.8 / 1000 persone all’anno.
Secondo una review del 2022 l’incidenza della SUDEP nella popolazione pediatrica sarebbe controversa, essendo riportata come 5 volte più bassa rispetto agli adulti in alcuni Studi e paragonabile a quella degli adulti in altri.
.
Meccanismi fisiopatologici del decesso da SUDEP
Meccanismi cardiaci
Il correlato anatomo-funzionale degli effetti cardiaci dell’epilessia risiederebbe nel sistema nervoso autonomo che esercita meccanismi di controllo discendente sui neuroni autonomici periferici che innervano il cuore.
La stimolazione ripetuta e incontrollata dei centri autonomici corticali e subcorticali (come insula, aree orbitofrontali e cingolata, amigdala e ipotalamo) durante le convulsioni provocherebbe infatti anomalie cardiocircolatorie, sotto forma di alterazioni della pressione arteriosa o della frequenza e del ritmo cardiaci, che potrebbero indurre morte improvvisa.
In alcuni pazienti deceduti per SUDEP sono stati dimostrati assottigliamento della corteccia mesiale e orbitofrontale e alterazioni degenerative insulari.
Alcuni Autori hanno anche postulato una disregolazione della connessione funzionale tra corteccia cingolata e orbitofrontale, amigdala e talamo che indurrebbe alterazioni del controllo periferico della funzione cardiaca con predisposizione alla SUDEP.
Una delle teorie più accreditate è che l’instabilità del sistema nervoso autonomo che deriva dall’attivazione comiziale di circuiti aberranti porti – convulsione dopo convulsione – ad alterazioni non solo funzionali, ma anche strutturali, dell’innervazione autonomica cardiaca con incremento del rischio di SUDEP negli epilettici di lunga data e/o con scarso controllo delle crisi convulsive.
Il ripetersi delle crisi determinerebbe infatti episodi ricorrenti di ipossiemia e scariche catecolaminergiche con conseguente tossicità cardiaca: il termine ‘cuore epilettico’ è stato adottato per descrivere il danno di perfusione cardiaca conseguente a epilessia cronica, con conseguente disfunzione meccanica e instabilità elettrica.
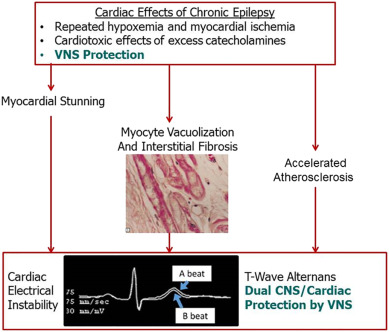
Schema concettuale che illustra il collegamento tra epilessia cronica e sviluppo di ‘cuore epilettico’ a causa della cardiotossicità delle catecolamine e degli episodi ripetuti di ipossiemia
.
Meccanismi respiratori
I testimoni spesso riportano difficoltà respiratorie terminali nei casi di morte da SUDEP.
I (limitati) dati relativi a pazienti con crisi comiziali in corso di monitoraggio strumentale respiratorio dimostrano l’insorgenza di apnea in fase ictale, spesso associata a bradicardia.
La ricorrenza di apnea o bradipnea e di conseguenza ipossia durante le convulsioni potrebbe giocare un ruolo nello sviluppo di SUDEP.
La prolungata desaturazione durante le crisi epilettiche è stata correlata con l’insorgenza di anomalie della ripolarizzazione (es. allungamento dell’intervallo QT), mentre alcune casistiche indicano che SpO2 inferiori a 80%-86% portano ad un aumento del rischio di SUDEP.
Se è vero che l’insufficienza respiratoria comiziale può dare avvio ad una cascata di eventi che termina con l’insorgenza di aritmie fatali, è stato anche postulato che possa esistere un meccanismo di morte da SUDEP primariamente respiratorio, poiché è stato osservato che, in alcuni pazienti, si verificano ipossia e ipercapnia anche a fronte di tachipnea ictale.
L’esame autoptico nelle morti SUDEP spesso rivela anomalie polmonari aspecifiche, tra le quali la più comune è rappresentata da intensa congestione con aumento del peso dei polmoni.
L’edema polmonare è frequente nelle crisi tonico-cloniche prolungate: sono stati proposti numerosi meccanismi che potrebbero spiegarne lo sviluppo; tra questi si annoverano una depressione respiratoria a livello centrale, output simpatico-simili sul tronco cerebrale, l’insorgenza di pressione toracica negativa da laringospasmo ictale o un aumento delle pressioni vascolari polmonari.
In uno studio del 2019 sui dati di monitoraggio strumentale di 87 pazienti nel corso di crisi comiziali è stato identificato il verificarsi di apnea centrale post ictale nel 22% dei casi. In particolare, le convulsioni ipniche sono state associate con ipossiemia più grave e prolungata rispetto a quelle diurne; la spiegazione potrebbe essere identificata nella riduzione durante il sonno della sensibilità chemorecettoriale associata ad un aumento delle resistenze delle alte vie aeree.
Queste potrebbero essere tra le ragioni di una più frequente ricorrenza della SUDEP durante il sonno.
Inoltre, è noto che vi sia una fase post-ictale di immobilità che potrebbe essere responsabile della ostruzione degli orifizi respiratori da lettereccio qualora il soggetto si trovi in posizione prona; quest’ultimo è effettivamente il decubito in cui più frequentemente sono rinvenuti i soggetti deceduti per SUDEP.
.
Meccanismi neuronali
È stata teorizzata anche la possibilità che la SUDEP sia favorita da una disfunzione dei neuromodulatori.
Studi sperimentali su modelli animali hanno documentato che una alterazione della trasmissione serotoninergica potrebbe avere un ruolo nella SUDEP, ipotesi che suggerirebbe delle analogie tra questa e la sudden infant death syndrome (SIDS).
Ciò che è noto è che la propagazione dell’onda elettrica comiziale nel tronco encefalo influisce sia sui neuroni serotoninergici del mesencefalo, che sono coinvolti nel sistema ascendente di arousal, sia su quelli del midollo allungato coinvolti nel controllo respiratorio e quindi potrebbe determinare un’alterazione su più livelli della funzione respiratoria.
La ricorrente eccessiva trasmissione elettrica neuronale lungo il midollo allungato potrebbe essere responsabile della sua perdita di volume rivelata dall’esame RMN in alcuni casi di SUDEP.
.
Gli studi su dati autoptici
La SUDEP è una sfida diagnostica, in primo luogo perché normalmente è un evento non testimoniato che occorre nottetempo.
La National Association of Medical Examiners in un position paper del 2018 sull’argomento risponde a 7 domande al fine di guidare il medico legale nei casi sospetti.
Tra i lavori su dati autoptici, è utile citare un ampio studio svolto a Istanbul che ha raccolto 20334 autopsie effettuate tra il 2007 e il 2011: tra queste, in 112 casi si trattava di pazienti con diagnosi di epilessia e la SUDEP è stata identificata come causa nel 35,7% dei casi (40 decessi sul totale). Il 95% di questi ultimi è stato sottoposto ad analisi tossicologiche: nel 33,5% dei casi era rilevata l’assenza di farmaci antiepilettici nel sangue.
Tra i pazienti identificati come deceduti per SUDEP, nel 72.9% dei casi vi erano segni esterni suggestivi per la ricorrenza di attacco epilettico in prossimità temporale rispetto al decesso, sotto forma di reperti aspecifici come escoriazioni o ecchimosi in regioni esposte ai traumatismi accidentali da caduta (aree protrudenti del volto, superfici estensorie delle articolazioni degli arti), petecchie congiuntivali, lacerazioni o infiltrazioni emorragiche della lingua.
Nel 92.5% dei casi vi erano segni micro e macroscopici di edema polmonare e nel 60% dei casi a questo si associava edema cerebrale.
Nel 47.5% dei casi di SUDEP inoltre il cuore aveva un peso sopra la norma, anche se il peso cardiaco era statisticamente maggiore nei soggetti della casistica deceduti per patologia cardiovascolare rispetto a quelli morti per SUDEP (p=0.002). L’esame istologico permetteva di osservare in entrambi i gruppi la presenza di ipertrofia dei miocardiociti e aree di sostituzione fibrosa del miocardio con frequenze che erano statisticamente maggiori per il gruppo di pazienti cardiovascolari rispetto a quelli epilettici.
In uno studio australiano del 2016 sulle morti diagnosticate come SUDEP in un periodo di 5 anni in Queensland è stato documentato un livello subterapeutico di anticonvulsivanti nel 55% dei casi, con morti avvenute perlopiù a domicilio (90%), di notte (70%), non testimoniate (87%), in decubito prono (74%), con segni di convulsioni perimortali (60%).
In uno studio retrospettivo condotto in Ontario (Canada) tra il 2014 e il 2016 due neurologi hanno esaminato i report autoptici e classificato le morti con i criteri di Nashef, per verificare l’appropriatezza diagnostica nelle morti attribuite a SUDEP. La concordanza diagnostica si riduceva nei casi più complessi e la SUDEP risultò sottodiagnosticata dai Medical Examiners nei pazienti più anziani.
Verduci e colleghi in uno studio pubblicato nel 2020 analogamente hanno documentato una discordanza tra le diagnosi attribuite dai Medici Legali e dagli Epilettologi sui medesimi casi, in quanto i coroner tendevano a favorire cause di morte non epilessia-relate, laddove erano presenti evidenze patologiche a carico di altri apparati.
Per un approfondimento sull’argomento vi rimandiamo alla review di Giussani e colleghi che esamina nel dettaglio le ipotesi eziopatogenetiche e diagnostiche di questa complessa patologia!
VUOI APPROFONDIRE QUESTO ARGOMENTO?
Leggi anche: Myocardial Bridging: variante anatomica o causa di morte improvvisa? e Morte asfittica nella folla: studio sperimentale su modello umano