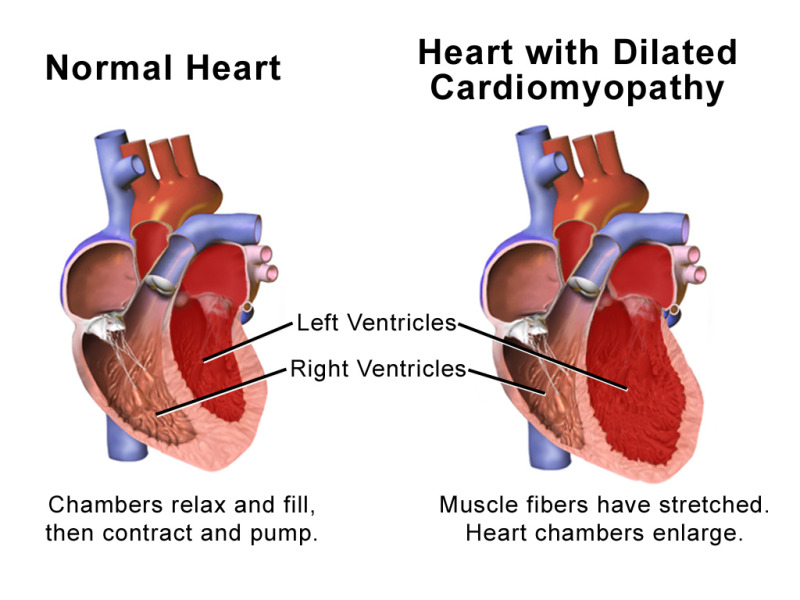
La cardiomiopatia alcolica è una malattia cardiaca causata dal consumo cronico di alcol caratterizzata da dilatazione ventricolare e compromissione della funzione cardiaca; essa rappresenta una delle principali cause di cardiomiopatia dilatativa non ischemica.
Approfondiamo questo tema, partendo dalle informazioni riportate nel capitolo dedicato su StatPearls, bookshelf costantemente aggiornato di PubMed, cui vi rimandiamo per una lettura completa – clicca qui.
Cardiotossicità cronica dell’alcol
La cardiotossicità a lungo termine dell’alcol è una causa riconosciuta di cardiomiopatia non ischemica e rappresenta ad oggi il 10% di tutti i casi di cardiomiopatie dilatative.
Il principale fattore di rischio è l’assunzione prolungata di ingenti quantità di alcol, vale a dire una storia di disturbo da consumo di alcol; tuttavia, non è stato identificato un valore limite di consumo di alcol rispetto allo sviluppo di cardiomiopatia dilatativa alcol-relata (Alcoholic Cardiomyopathy, ACM).
Non è stato nemmeno identificato un tempo minimo di esposizione perché si sviluppi la malattia. E’ noto che un consumo di alcol pari o superiore a 80 g/die per più di 5 anni aumenta significativamente il rischio, tuttavia non tutti gli etilisti cronici sviluppano la ACM.
La correlazione tra consumo etilico e reperti ecocardiografici è stata indagata su un campione di 2368 adulti con follow-up a lungo termine durante lo studio CARDIA pubblicato su JAMA Cardiology nel 2020: è stata documentata una associazione diretta tra assunzione di alcol e alterazioni patologiche della struttura ventricolare. In particolare, l’aumento del consumo di alcol era associato a una ipertrofia di parete ventricolare sinistra e ad un aumento del volume telediastolico del ventricolo sinistro nell’arco di 20 anni.
Epidemiologia
Negli Stati Uniti l’incidenza della ACM è stimata all’1-2% tra tutti i forti consumatori di alcol; la prevalenza tra coloro che frequentano le unità sanitarie di aiuto alla disintossicazione sarebbe tra il 21 e il 32%.
In realtà, probabilmente il fenomeno è sottostimato per la mancanza di dati clinici relativi a una buona parte degli eitlisti.
L’identikit del paziente affetto da ACM è un soggetto di sesso maschile, di età compresa tra 30 e 55 anni, con una storia significativa di consumo di alcol per più di 10 anni.
Le donne costituiscono circa il 14% dei casi, ma sviluppano la malattia per livelli di esposizione all’alcol inferiori a quelli necessari per gli uomini.
I tassi di mortalità sono più alti nei maschi rispetto alle femmine e più elevati nei neri rispetto ai bianchi.
Le interazioni tra fattori genetici e non genetici, l’esposizione ad altre sostanze cardiotossiche o le carenze di minerali come la tiamina giocano un ruolo importante nel determinare la progressione della cardiomiopatia alcolica.
Eziologia
E’ noto da tempo che l’alcol e i suoi metaboliti sono cardiotossici; la depressione miocardica secondaria all’abuso di alcol è inizialmente reversibile, ma se prolungata porta a disfunzioni irreversibili.
Sono stati ipotizzati diversi meccanismi fisiopatologici nello sviluppo della ACM. Alla base dell’insorgenza della malattia vi sarebbero la tossicità dell’alcol sui mitocondri e la sua capacità di indurre stress ossidativo, apoptosi, modifiche della struttura di actina e miosina e alterazioni dell’omeostasi del calcio.
L’esposizione per consumo di alcol provoca infatti un aumento della frammentazione mitocondriale per incremento dei livelli delle specie reattive dell’ossigeno (ROS) nei miociti, con ossidazione di lipidi, proteine e DNA.
Queste alterazioni strutturali intracellulari causerebbero l’attivazione di meccanismi compensatori in risposta alla disfunzione cardiaca, come il sistema renina-angiotensina-aldosterone e l’aumento del segnale simpatico e dei peptidi natriuretici cerebrali, che a loro volta sarebbero responsabili di un aumento del precarico, della dilatazione del ventricolo sinistro e della diminuzione della gittata cardiaca che contribuiscono alla manifestazione clinica dell’ACM.
Attualmente la ricerca si sta concentrando sul ruolo delle caratteristiche genetiche individuali nel determinare lo sviluppo della cardiomiopatia. La patogenesi dell’ACM comporta infatti l’interazione tra fattori geneticamente correlati, come i sottotipi HLA o l’allele dell’enzima alcol deidrogenasi, e fattori “ambientali”, tra cui la carenza di tiamina e l’esposizione a varie sostanze direttamente tossiche per le cellule cardiache.
Per esempio, uno studio di Ware et al. ha suggerito che varianti troncate del gene della titina (TTNtv) potrebbero avere un ruolo sullo sviluppo e sulla gravità della ACM.
Istopatologia
Le alterazioni strutturali cellulari più comuni includono alterazioni del reticolo mitocondriale, formazione di ammassi di mitocondri e scomparsa delle giunzioni inter-mitocondriali.
Si possono osservare anche alterazioni dell’attività enzimatica, tra cui la diminuzione dell’attività degli enzimi mitocondriali di riduzione dell’ossigeno, l’incremento dell’assorbimento degli acidi grassi e l’aumento dell’attività degli enzimi lisosomiali/microsomiali.
Sintomatologia
La disfunzione diastolica è il segno più precoce dell’ACM e si riscontra in circa il 30% dei pazienti con una storia di abuso cronico di alcol, anche in assenza di disfunzione sistolica o di ipertrofia del ventricolo sinistro.
La cardiomiopatia alcolica clinicamente scompensata si presenta con segni e sintomi di insufficienza cardiaca congestizia: dispnea di gravità variabile, ortopnea/dispnea parossistica notturna, cardiopalmo, episodi sincopali di natura tachiaritmica, anoressia, atrofia muscolare, debolezza, edemi periferici, ecc.
Possono essere coesistere anche altre alterazioni patologiche legate all’abuso di alcol: epatopatia, carenza di folati, aumento del rischio di emorragie da insufficienza epatica, malnutrizione, neuropatia periferica e condizioni neurologiche come la sindrome di Wernicke-Korsakoff.
Diagnosi
La diagnosi di cardiomiopatia alcolica è aspecifica. Non esistono biomarcatori istologici o immunologici patognomonici che consentano una diagnosi diretta di cardiomiopatia indotta da alcol.
In primo luogo, deve essere presente una storia personale di etilismo e devono essere escluse altre eziologie che potrebbero giustificare lo sviluppo di una cardiopatia dilatativa (per es. malattia coronarica/cardiopatia ischemica).
Esami di laboratorio, come il volume corpuscolare medio e i livelli di GGT, AST e ALT, possono essere utili come prova indiretta a supporto dell’uso di alcol..
Per quanto riguarda gli esami di imaging, è indicata l’esecuzione di:
- ECG: si può osservare una molteplicità di alterazioni, tra cui contrazioni atriali o ventricolari premature, tachicardie sopraventricolari, blocchi atrioventricolari, blocchi di branca, prolungamento del QT, alterazioni aspecifiche del tratto ST e dell’onda T e onde Q anomale;
- RX torace: la silhouette cardiaca può essere allargata e si possono riscontrare congestione vascolare polmonare e versamento pleurico.
Pertanto, soddisfatti i criteri anamnestico e di esclusione di altre cause, la diagnosi di cardiomiopatia alcolica è raggiunta se l’ecocardiogramma evidenza:
Prognosi
La cardiomiopatia dilatativa indotta dall’alcol ha una prognosi migliore rispetto alla cardiomiopatia indotta da ischemia. La presenza di fibrillazione atriale e di allungamento del QRS > 120 ms e la mancata assunzione di terapia farmacologica specifica sono fattori sfavorevoli.
I dati suggeriscono che i pazienti che hanno smesso di bere con successo hanno un numero ridotto di ricoveri e un miglioramento dei parametri ecocardiografici.
È stato dimostrato che la sopravvivenza a lungo termine è direttamente associata alla quantità e alla durata dell’uso di alcol. Ovviamente, i pazienti che continuano a bere hanno una prognosi peggiore.
A seconda dell’entità del disturbo alcolico, si registrano tassi di mortalità del 40-80% a 10 anni.
VUOI SCOPRIRE DI PIU’?
Leggi anche: Morte cardiaca improvvisa dopo assunzione di alcol e Riscontri diagnostici e cardiomiopatie su base genetica